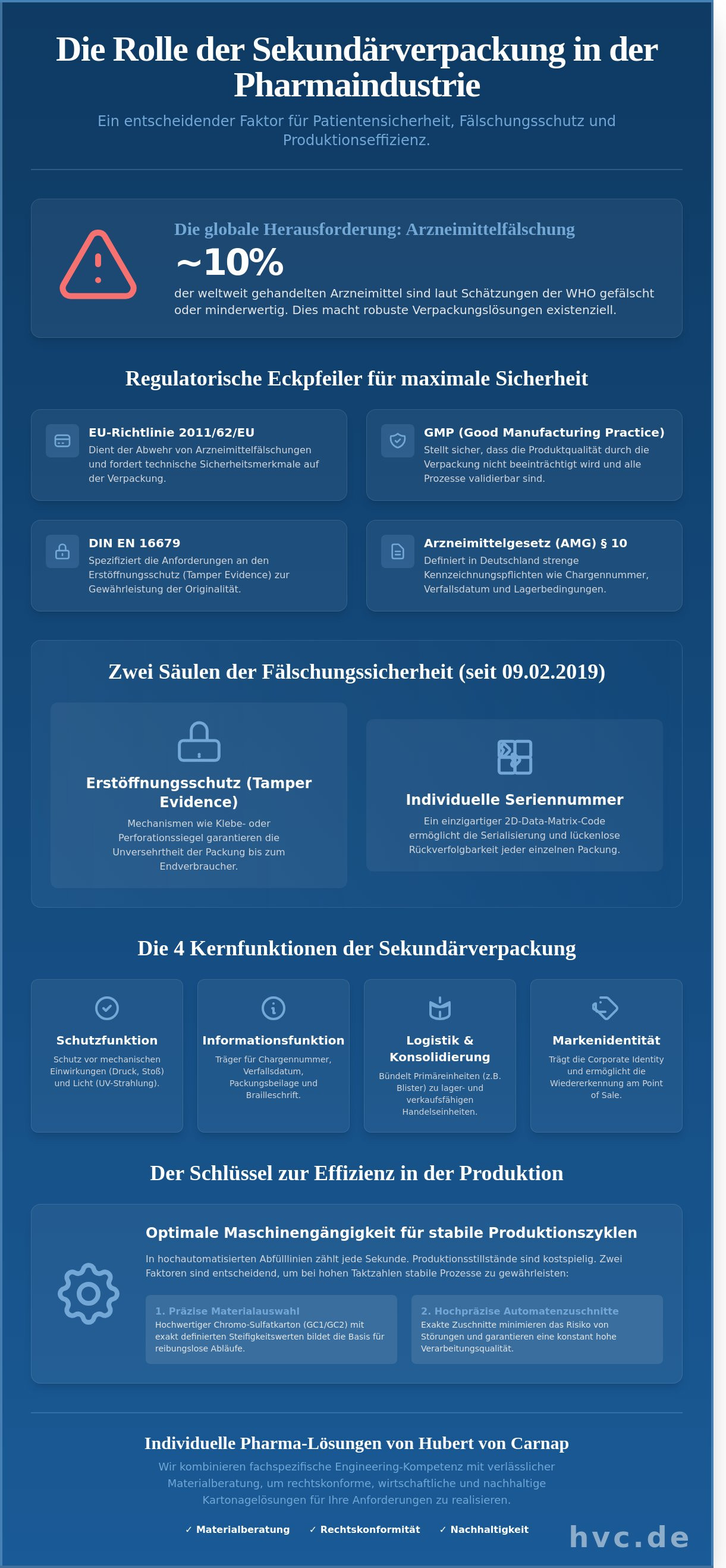
Rund 10 % der weltweit gehandelten Arzneimittel werden laut Schätzungen der Weltgesundheitsorganisation (WHO) als gefälscht oder minderwertig eingestuft, was die strikte Einhaltung der EU-Richtlinie 2011/62/EU für Hersteller zu einer existenziellen Verpflichtung macht. Sicherlich ist Ihnen bewusst, dass die Sekundärverpackung Pharma längst über die reine Schutzfunktion hinausgeht und als zentrales Element der Patientensicherheit sowie der logistischen Integrität fungiert. Die Komplexität der Anforderungen steigt stetig, da sowohl die fälschungssichere Versiegelung nach DIN EN 16679 als auch eine maximale Effizienz in hochautomatisierten Abfülllinien gleichzeitig gewährleistet werden müssen.
In diesem Beitrag erfahren Sie alles über die kritische Rolle der Sekundärverpackung für die Arzneimittelsicherheit, die aktuellen regulatorischen Anforderungen und die Parameter für hocheffiziente Verpackungsprozesse. Es wird detailliert dargelegt, wie durch eine präzise Materialauswahl und optimierte Automatenzuschnitte die Maschinengängigkeit signifikant erhöht und das Risiko kostspieliger Produktionsstillstände minimiert wird. Wir beleuchten zudem die Bedeutung einer verlässlichen Materialberatung, die als Basis für die Entwicklung rechtskonformer und wirtschaftlich tragfähiger Lösungen dient, damit Ihre Produktionszyklen auch bei hohen Taktzahlen stabil bleiben.
Wichtigste Erkenntnisse
- Verstehen Sie die essenzielle Schutzfunktion der Sekundärverpackung gegen Licht und mechanische Belastungen zur Sicherung der pharmazeutischen Produktintegrität.
- Erfahren Sie, wie die strikte Einhaltung von GMP-Standards und der EU-Richtlinie 2011/62/EU eine lückenlose Fälschungssicherheit in der Lieferkette gewährleistet.
- Optimieren Sie Ihre Produktionszyklen durch den Einsatz hochpräziser Maschinenzuschnitte, die speziell für die Anforderungen der sekundärverpackung pharma entwickelt wurden.
- Differenzieren Sie präzise zwischen Primär- und Sekundärverpackungen hinsichtlich Materialspezifika und regulatorischer Anforderungen für eine effiziente Prozessplanung.
- Nutzen Sie fachspezifische Engineering-Kompetenz zur Realisierung nachhaltiger Kartonagelösungen, die ökologische Ansprüche mit technischer Präzision vereinen.
Definition und Funktionen der Sekundärverpackung in der Pharmazeutik
Die Sekundärverpackung pharma definiert sich als die äußere Umhüllung, welche das primär verpackte Arzneimittel umschließt, ohne dabei eine direkte stoffliche Grenzfläche zum Wirkstoff zu bilden. Ihre primäre Aufgabe besteht in der Konsolidierung einzelner Primäreinheiten, wie Blisterstreifen oder Ampullen, zu logistischen und verkaufsfähigen Handelseinheiten. Die technische Ausführung erfolgt meist durch Faltschachteln aus hochwertigem Chromo-Sulfatkarton (GC1 oder GC2), der spezifische Steifigkeitswerte aufweist, um den Inhalt vor mechanischen Einwirkungen während der automatisierten Konfektionierung und des Transports zu schützen.
Neben der Schutzfunktion gegenüber Druckbelastungen übernimmt die Sekundärverpackung kritische Barriereaufgaben. Sie dient als Lichtschutz für photosensible Substanzen, die durch UV-Strahlung chemische Degradationsprozesse erfahren könnten. Die Informationsfunktion ist ein weiteres Kernmerkmal. Hierbei werden gesetzlich vorgeschriebene Kennzeichnungen sowie die Blindenschrift (Braille) integriert, um die Barrierefreiheit gemäß den Anforderungen der Patientensicherheit zu gewährleisten. Im kommerziellen Kontext fungiert die Gestaltung als Träger der Corporate Identity. Eine präzise Markenführung am Point of Sale in der Apotheke ermöglicht die schnelle Wiedererkennung durch das pharmazeutische Fachpersonal und den Endverbraucher, was die Therapietreue indirekt stützen kann.
Warum die Sekundärverpackung für die Patientensicherheit kritisch ist
Die Integrität der Primärverpackung wird durch die äußere Hülle während der gesamten Lieferkette sichergestellt. Durch passgenaue Konstruktionen und Inlays werden Glasbruch oder Blisterbeschädigungen minimiert. Ein präzises grafisches Design verhindert Verwechslungen zwischen unterschiedlichen Dosierungsstärken. Zudem ist die Sekundärverpackung der gesetzlich vorgeschriebene Ort für die Unterbringung der Packungsbeilage, deren Vorhandensein für die korrekte Anwendung des Medikaments durch den Patienten unentbehrlich ist.
Rechtliche Grundlagen und Kennzeichnungspflichten
In Deutschland definiert das Arzneimittelgesetz (AMG) in § 10 die strengen Anforderungen an die äußere Umhüllung. Jede Sekundärverpackung pharma muss zwingend Angaben zur Chargennummer, zum Verfalldatum und zu spezifischen Lagerungsbedingungen enthalten. Die Lesbarkeit dieser Daten muss durch hochresistente Druckverfahren über den gesamten Lebenszyklus des Produkts gewahrt bleiben. Gemäß der EU-Richtlinie 2011/62/EU ist zudem ein Erstöffnungsschutz sowie ein 2D-Data-Matrix-Code zur Serialisierung und Rückverfolgbarkeit obligatorisch.
Regulatorische Anforderungen: GMP und Fälschungssicherheit
Die Einhaltung der Good Manufacturing Practice (GMP) bildet das regulatorische Fundament für die pharmazeutische Industrie. Jede sekundärverpackung pharma muss so konzipiert sein, dass sie nicht nur logistische Funktionen erfüllt, sondern auch den strengen Vorgaben der EU-Richtlinie 2011/62/EU entspricht. Diese Richtlinie dient der Abwehr von Arzneimittelfälschungen und verlangt die Implementierung technischer Sicherheitsmerkmale. Die Einhaltung der GMP-Anforderungen für Verpackungsmaterialien stellt sicher, dass die Qualität des Arzneimittels durch die äußere Hülle nicht beeinträchtigt wird und alle Prozesse validierbar sind. Seit dem 9. Februar 2019 müssen verschreibungspflichtige Medikamente in der EU Merkmale zur Erkennung von Manipulationen sowie eine individuelle Seriennummer tragen. Die Validierung der Verpackungsprozesse ist hierbei ein kritischer Schritt, um sicherzustellen, dass die Integrität der Primärverpackung während des gesamten Sekundärverpackungsvorgangs gewahrt bleibt. Dies erfordert eine hochpräzise Abstimmung zwischen Materialauswahl, Drucktechnik und Software-Integration, um eine lückenlose Rückverfolgbarkeit in der legalen Lieferkette zu gewährleisten.
Erstöffnungsschutz: Mechanismen für garantierte Originalität
Der Erstöffnungsschutz (Tamper Evidence) garantiert die Unversehrtheit der Packung bis zum Endverbraucher. Technische Lösungen wie verleimte Laschen oder spezifische Perforationsmuster machen jeden Öffnungsversuch irreversibel sichtbar. Alternativ kommen Sicherheitsetiketten (Anti-Tampering Seals) zum Einsatz, die beim Ablösen die Kartonoberfläche zerstören. Die Materialspezifikation dieser Siegel muss exakt auf die Oberflächenspannung des Kartons abgestimmt sein, um eine zuverlässige Funktion unter variierenden klimatischen Bedingungen und Lagerungszeiten sicherzustellen.
Serialisierung und Datenmanagement
Die Serialisierung erfolgt über einen 2D-DataMatrix-Code, der GTIN, Seriennummer, Charge und Verfallsdatum speichert. Für die maschinelle Lesbarkeit ist ein hoher Druckkontrast auf der sekundärverpackung pharma erforderlich, was spezifische Anforderungen an den Weißgrad und die Saugfähigkeit des Substrats stellt. Integrierte Kamerasysteme prüfen die Druckqualität in Echtzeit gemäß ISO/IEC 15415. Fehlerhafte Einheiten werden durch pneumatische Systeme automatisch ausgeschleust, um die Prozesssicherheit bei hohen Produktionsgeschwindigkeiten von oft über 300 Einheiten pro Minute zu wahren.
Primär- vs. Sekundärverpackung: Ein struktureller Vergleich
Die Differenzierung zwischen den Verpackungsebenen basiert primär auf der physikalischen Nähe zum pharmazeutischen Wirkstoff. Während die Primärverpackung, etwa eine Ampulle aus Borosilikatglas oder ein PVC/PVDC-Blister, eine unmittelbare Stoffbarriere bildet, übernimmt die sekundärverpackung pharma die strukturelle Integrität der Verkaufseinheit. Diese Trennung ist regulatorisch zwingend, da Materialien mit direktem Produktkontakt strengen Migrationsprüfungen unterliegen. Die Sekundärschicht schützt das Primärbehältnis vor mechanischer Einwirkung und dient als Träger für gesetzlich vorgeschriebene Sicherheitsmerkmale wie den Data-Matrix-Code oder Originalitätsverschlüsse.
Das Zusammenwirken beider Ebenen ist entscheidend für die Stabilität des Medikaments. Eine mangelhafte Barriereleistung der äußeren Hülle kann die Lichtexposition erhöhen, was bei photosensitiven Substanzen zu einer Degradation des Wirkstoffs führt. Hierbei müssen Hersteller strikte Regulatorische Anforderungen an die Verpackung erfüllen, die eine lückenlose Kontrolle und Dokumentation der Verpackungsprozesse vorschreiben. Die technische Auslegung der Sekundärverpackung orientiert sich dabei an der Logistikkette und den Anforderungen der automatisierten Abfüllanlagen.
Die Hierarchie der pharmazeutischen Verpackung
Die Verpackungsstruktur in der pharmazeutischen Industrie ist in drei funktionale Ebenen unterteilt, die jeweils spezifische Schutzaufgaben wahrnehmen:
- Primärverpackung: Diese Ebene bildet die direkte Barriere. Sie besteht aus Materialien wie Glas der hydrolytischen Klasse I, Aluminiumfolien oder speziellen Kunststoffen. Die Abfüllung erfolgt unter Reinraumbedingungen, um die Sterilität zu gewährleisten.
- Sekundärverpackung: Die sekundärverpackung pharma bündelt die Primärpackmittel zu einer Handelseinheit. Sie besteht meist aus hochwertigem Zellstoffkarton und bietet Raum für die Packungsbeilage sowie Identifikationsmerkmale. Sie schützt zudem vor UV-Strahlung und mechanischem Druck.
- Tertiärverpackung: Diese dient ausschließlich der Logistik. Wellpappkartons oder Paletten sichern die Ware während des Transports gegen Transportschäden und ermöglichen eine effiziente Lagerhaltung in Großhandelsstrukturen.
Materialwahl für pharmazeutische Faltschachteln
Die Auswahl des Kartons für die Sekundärverpackung wird durch die Anforderungen der Hochgeschwindigkeits-Abfülllinien bestimmt. Hier kommen vorwiegend GC1 und GC2 Chromokartons zum Einsatz. Diese Frischfasermaterialien zeichnen sich durch eine hohe Biegesteifigkeit und eine exzellente Bedruckbarkeit aus. Eine glatte Oberfläche ist essenziell, um die Lesbarkeit von kleinteiligen Texten und variablen Daten wie Chargennummern und Verfallsdaten mit einer Fehlerrate von nahezu 0 % sicherzustellen.
Im Gegensatz dazu wird GD2 Recyclingkarton aufgrund potenzieller Migrationsrisiken von Mineralölrückständen seltener für verschreibungspflichtige Medikamente verwendet. Sein Einsatz beschränkt sich oft auf unkritische OTC-Produkte oder Nahrungsergänzungsmittel. Für automatisierte Prozesse sind Spezialkartonagen mit optimierten Reibungswerten erforderlich. Diese gewährleisten, dass die Schachteln bei Taktraten von über 400 Einheiten pro Minute präzise aufgerichtet und befüllt werden können. Die Materialkonstante spielt eine zentrale Rolle für die Gesamtanlageneffektivität (OEE) in der Produktion. Ähnliche Anforderungen an die Maschinengängigkeit unter anspruchsvollen Umgebungsbedingungen stellen sich auch bei der Verpackung gekühlter Lebensmittel, wo Feuchtigkeitsresistenz und präzise Materialeigenschaften gleichermaßen entscheidend sind.
Effizienz in der Produktion: Automatenzuschnitte und Maschinengängigkeit
Die Wirtschaftlichkeit einer pharmazeutischen Verpackungslinie hängt unmittelbar von der Präzision der Automatenzuschnitte ab. Bei Hochgeschwindigkeits-Anlagen, die oft bis zu 400 Einheiten pro Minute verarbeiten, führen bereits minimale Abweichungen in der Rillung oder der Ausbrechqualität zu kostspieligen Stillstandszeiten. Eine exakt kalibrierte Sekundärverpackung Pharma muss einen definierten Rückstellwiderstand aufweisen, damit das Aufrichten der Schachtel in der Maschine ohne mechanischen Widerstand erfolgt. Wenn die Rilllinien nicht präzise gesetzt sind, entstehen asymmetrische Spannungen, die den reibungslosen Einschub des Primärpackmittels blockieren.
Neben der mechanischen Konstruktion beeinflussen externe Faktoren die Laufleistung massiv. Karton ist als hygroskopisches Material empfindlich gegenüber Schwankungen der Umgebungstemperatur und Luftfeuchtigkeit. Eine Lagerung außerhalb des optimalen Bereichs von 18 bis 22 Grad Celsius bei einer relativen Luftfeuchtigkeit von 50 Prozent verändert die Faserstruktur. Dies führt oft zu einer Beeinträchtigung der Planlage (Curl), wodurch die Vakuumsauger der Anlage die Zuschnitte nicht mehr zuverlässig aus dem Magazin entnehmen können. Die Einhaltung dieser klimatischen Parameter ist daher für eine konstante Maschinengängigkeit zwingend erforderlich.
Konstruktion für automatisierte Prozesse
Die technische Auslegung der Faltschachteln orientiert sich primär an standardisierten Formaten nach dem ECMA-Code, wie etwa der Bauform A20.20. Dennoch erfordern moderne Hochleistungs-Kartonierer oft individuelle Sonderkonstruktionen, um die Staub- und Einstecklaschen für automatische Verschließer zu optimieren. Im Fokus steht hierbei die Reduzierung von Reibungswerten und die exakte Positionierung der Einsteckschlitze. Während der Entwicklungsphase werden Toleranzen von weniger als 0,1 Millimetern definiert. Diese Präzision im Musterbau stellt sicher, dass die spätere Serienfertigung keine Abweichungen aufweist, die den automatisierten Prozess stören könnten.
Qualitätssicherung bei Automatenzuschnitten
Zur Sicherstellung einer stabilen Produktion sind kontinuierliche In-Prozess-Kontrollen unumgänglich. Hierbei wird die Einhaltung der Maße gemäß DIN ISO 2768-m überwacht, um eine gleichbleibende Qualität über die gesamte Losgröße zu garantieren. Ein wesentlicher Prüfpunkt ist die Planlage der flachliegenden Zuschnitte. Nur eine absolut plane Oberfläche verhindert Maschinenstopps durch fehlerhafte Vereinzelung. Jede Fertigungscharge wird lückenlos dokumentiert, was eine vollständige Rückverfolgbarkeit bis zum Rohmaterialhersteller ermöglicht. Diese Datenintegrität ist ein zentraler Bestandteil der Qualitätssicherung in der pharmazeutischen Lieferkette.
Für die Optimierung Ihrer Produktionsprozesse bietet eine fundierte technische Beratung die notwendige Grundlage. Erfahren Sie mehr über unsere hochpräzisen Lösungen für die pharmazeutische Sekundärverpackung.
Individuelle Pharma-Lösungen von Hubert von Carnap
Hubert von Carnap agiert als strategischer Partner für Unternehmen, die über die reine Beschaffung hinausgehende Anforderungen an ihre Packmittel stellen. Der Fokus liegt auf der Entwicklung von Lösungen, die exakt auf die hochspezifischen Anforderungen der mittelständischen Pharmaindustrie zugeschnitten sind. Ein Full-Service-Ansatz deckt sämtliche Phasen ab: von der initialen Konzeption über die präzise Konstruktion bis hin zur hochmodernen Fertigung in Deutschland. Diese lokale Wertschöpfung garantiert eine strikte Einhaltung der GMP-konformen Produktionsbedingungen und sichert kurze Reaktionszeiten bei kurzfristigen Bedarfsänderungen.
Die Realisierung einer sekundärverpackung pharma erfordert eine tiefe Kenntnis der regulatorischen Rahmenbedingungen, wie sie in der Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) festgeschrieben sind. Hubert von Carnap verbindet diese juristische Sicherheit mit technischer Innovationskraft. Das Ergebnis sind Pharmakartonagen, die sowohl ökologische Kriterien erfüllen als auch den Schutz des Füllguts während der gesamten Logistikkette gewährleisten. Langjährige Expertise in der Zusammenarbeit mit spezialisierten Herstellern bildet das Fundament für eine Prozesssicherheit, die Ausfallzeiten an den Abfülllinien der Kunden minimiert.
Verpackungsentwicklung und Prototyping
Die technische Validierung neuer Verpackungskonzepte erfolgt durch einen spezialisierten Musterbau. Hier entstehen physische Prototypen, die Kunden zur Funktionsprüfung auf ihren automatisierten Verpackungsanlagen nutzen. Diese Testläufe sind essenziell, um die Lauffähigkeit und Aufrichteeigenschaften unter Realbedingungen zu bestätigen. Die Materialberatung adressiert dabei gezielt Parameter wie den Stapelstauchwiderstand und die Eignung für thermotransfer- oder laserbasierte Codierungen. Zudem werden komplexe Anforderungen wie integrierte Inlays oder Halterungen konstruktiv so gelöst, dass sie die Primärpackmittel fixieren und mechanische Einwirkungen abfedern. Dies reduziert die Bruchrate bei empfindlichen Glasbehältnissen deutlich.
Nachhaltigkeit in der Pharmaverpackung
Ökologische Zielsetzungen werden durch den konsequenten Einsatz von FSC- und PEFC-zertifizierten Materialien verfolgt. Die Konstruktionsabteilung minimiert den Materialverbrauch durch intelligente Nesting-Verfahren und eine Reduktion der Verschnittmengen im Stanzprozess. Eine optimierte sekundärverpackung pharma zeichnet sich dadurch aus, dass sie bei minimalem Eigengewicht maximale Schutzfunktion bietet. Die Produktion am Standort Deutschland ermöglicht eine CO2-optimierte Wertschöpfungskette durch kurze Transportwege zu den Abfüllbetrieben. Durch den Einsatz moderner, energieeffizienter Maschinenparks wird der ökologische Fußabdruck pro Verpackungseinheit systematisch gesenkt, ohne die geforderte Materialfestigkeit oder die Veredelungsqualität zu beeinträchtigen.
Zukunftssichere Prozessstabilität durch technische Präzision
Die Auswahl der optimalen sekundärverpackung pharma ist maßgeblich für die Einhaltung regulatorischer Standards wie der EU-Richtlinie 2011/62/EU zur Fälschungssicherheit. Technische Spezifikationen und die exakte Maschinengängigkeit der Kartonagen bestimmen die Effizienz hochautomatisierter Abfülllinien unmittelbar. Hubert von Carnap stützt sich auf eine über 150-jährige Expertise in der Kartonagen-Produktion, um diese komplexen Anforderungen prozesssicher zu erfüllen. Die Fertigung erfolgt unter Einhaltung strengster Qualitätsmaßstäbe sowie aktueller GMP-Vorgaben ausschließlich an Standorten in Deutschland. Hierbei liegt der Fokus auf hochpräzisen Automatenzuschnitten, die Stillstandzeiten in der Produktion minimieren und eine reibungslose Verarbeitung gewährleisten.
Durch die konsequente Ausrichtung auf technische Genauigkeit und zertifizierte Prozesse werden Fehlerquoten gesenkt und die Patientensicherheit nachhaltig gestärkt. Vertrauen Sie auf eine Zusammenarbeit, die durch fundiertes Engineering und jahrzehntelange Branchenkenntnis im B2B-Sektor geprägt ist. Sie erhalten Komponenten, die exakt auf Ihre individuellen Spezifikationen und Anlagenparameter abgestimmt sind. Optimieren Sie Ihre pharmazeutische Wertschöpfungskette mit Lösungen, die höchste funktionale Zuverlässigkeit und langlebige Qualität bieten.
Spezifizierte Pharma-Verpackungen bei HVC anfragen
Häufig gestellte Fragen zur pharmazeutischen Verpackung
Was ist der Unterschied zwischen Primär- und Sekundärverpackung?
Die Primärverpackung steht in direktem physischem Kontakt mit dem Arzneimittel, während die Sekundärverpackung als zusätzliche äußere Schutzhülle fungiert. Zu den Primärpackmitteln zählen Blister, Ampullen oder Vials, welche die chemische Stabilität und Sterilität des Inhalts sichern. Die Sekundärverpackung übernimmt primär logistische Aufgaben, schützt vor mechanischen Einflüssen und dient als Träger für gesetzlich vorgeschriebene Kennzeichnungen sowie die Packungsbeilage.
Welche Informationen müssen zwingend auf einer Pharma-Sekundärverpackung stehen?
Gemäß § 10 des Arzneimittelgesetzes (AMG) müssen Angaben wie Produktname, Wirkstärke, Darreichungsform, Chargenbezeichnung und Verfalldatum dauerhaft lesbar aufgebracht sein. Zusätzlich sind der Name des pharmazeutischen Unternehmers, die Zulassungsnummer und spezifische Warnhinweise erforderlich. Seit Inkrafttreten der EU-Richtlinie 2011/62/EU ist zudem ein individuelles Erkennungsmerkmal in Form eines 2D-DataMatrix-Codes zur Serialisierung jeder einzelnen Packung zwingend vorgeschrieben.
Warum ist die Maschinengängigkeit bei Pharma-Kartonagen so wichtig?
Die Maschinengängigkeit bestimmt die Effizienz automatisierter Verpackungslinien, die oft Taktraten von über 400 Einheiten pro Minute erreichen. Geringfügige Abweichungen in der Kartonsteifigkeit oder unpräzise Rillungen führen zu sofortigen Stillstandzeiten und erhöhen die Ausschussrate im Produktionsprozess. Eine exakte Abstimmung der Oberflächenreibung und der mechanischen Widerstandsfähigkeit ist für das fehlerfreie Aufrichten der Schachteln in der Hochleistungsanlage technisch unverzichtbar für eine stabile Ausbringungsmenge.
Wie wird die Fälschungssicherheit bei Faltschachteln technisch umgesetzt?
Die technische Umsetzung der Fälschungssicherheit basiert auf der Kombination einer eindeutigen Serialisierung mit einem physischen Erstöffnungsschutz. Ein aufgedruckter DataMatrix-Code enthält eine weltweit einmalige Seriennummer, die vor der Abgabe in der Apotheke gegen ein zentrales Datenbanksystem geprüft wird. Ergänzend machen mechanische Vorrichtungen wie Siegeletiketten oder spezielle Klebeverschlüsse jede Manipulation an der Packung für den Anwender sofort sichtbar.
Welche Kartonarten eignen sich am besten für Sekundärverpackungen?
Für die Sekundärverpackung Pharma werden überwiegend gestrichene Chromokartons der Kategorien GC1 oder GC2 eingesetzt. Diese Materialien verfügen über ein Flächengewicht zwischen 250 und 350 g/m² und bieten die erforderliche Biegesteifigkeit für den Schutz empfindlicher Primärpackmittel. Die glatte Oberflächenbeschaffenheit gewährleistet zudem eine präzise Bedruckbarkeit technischer Codes, was für die maschinelle Lesbarkeit der Serialisierungsdaten von entscheidender Bedeutung ist.
Was bedeutet Tamper Evidence im Kontext von Pharmaverpackungen?
Tamper Evidence bezeichnet technische Merkmale, die eine unbefugte Erstöffnung der Sekundärverpackung Pharma irreversibel und deutlich erkennbar anzeigen. Diese Sicherheitsvorrichtung ist durch die delegierte Verordnung (EU) 2016/161 für den Großteil der verschreibungspflichtigen Medikamente gesetzlich vorgeschrieben. In der Praxis wird dies durch spezielle Leimverschlüsse, Perforationen oder Sicherheitssiegel realisiert, die beim ersten Öffnungsvorgang zerstört werden und so die Integrität der Lieferung bestätigen.
Können Pharmaverpackungen nachhaltig produziert werden?
Eine nachhaltige Produktion wird durch den Einsatz von FSC- oder PEFC-zertifizierten Frischfasern und die konsequente Reduktion der Materialstärken erreicht. In Deutschland erzielen papierbasierte Verpackungen eine Recyclingquote von über 85 Prozent, was die Kreislauffähigkeit des Materials unterstreicht. Innovative Konstruktionsverfahren ermöglichen es zudem, das Gesamtgewicht der Kartonagen um bis zu 12 Prozent zu senken, ohne die notwendige Stapelstabilität oder Schutzfunktion im Transportprozess zu gefährden.
Welche Rolle spielt die Blindenschrift auf der Sekundärverpackung?
Die Blindenschrift ist laut § 10 Abs. 1b AMG eine verpflichtende Anforderung, um sehbehinderten Patienten die sichere Identifikation des Arzneimittels zu ermöglichen. Der Produktname muss in Braille-Schrift auf der Außenhülle aufgebracht sein, wobei die Norm DIN EN 15823 die exakten Parameter für Punkthöhe und Abstände festlegt. Diese Prägung erfolgt üblicherweise während des Stanzvorgangs in der Druckerei und erfordert eine hohe Präzision, um die Lesbarkeit über den gesamten Lebenszyklus der Packung zu erhalten.


